如何解决无菌采血管设备常见故障,提升检测准确性
如何解决无菌采血管设备常见故障,提升检测准确性
一、从“管、架、机”三端排查,先把基础问题掐死在萌芽
做了这么多年检验,我越来越清楚一点:无菌采血管相关故障,80%出在“管不行、架不行、机不懂人”。先说采血管本身。最典型的故障是负压不足、添加剂比例异常和批次差异大,表现为采血量不够、凝血时间异常、溶血率飙升。我的做法是:每换一批管,必须做“到货验证”——抽查同批号10支以上,记录实采血量、是否有气泡、凝块情况,并和仪器质控结果对照,一旦发现批次偏差,宁愿整批退货也不冒险。采血架的问题多在“混装”和“交叉污染”,很多科室习惯把不同用途的管随意堆放,结果是护士拿错管型,凝血管当生化管用,这种错误你在仪器上根本看不出来,只能从结果“离谱”来猜。我要求的是:架位固定、颜色固定、标签固定,培训时让护士闭眼凭手感就能摸出哪一种管,这个训练很管用。至于分析仪,常见故障是识别不到条码、样本量不足报警、检测通道污染。这里我有个硬性要求:每天接收标本前,必须做一次“空跑+模拟样本”自检,确认条码识别、混匀功能和探针吸样都正常,再正式上样。这套“管、架、机”三端排查流程坚持下来,能直接干掉一半的低级错误。
关键要点一:每批采血管到货前置验证
要想检测结果稳定,先别迷信“厂家质检”,得有自己的底线标准。我在科室制定了一份《采血管到货验证记录表》,包括批号、有效期、外观、采血量、凝血情况、溶血情况、与上批结果可比性等项目。到货后由固定两人负责抽样,按项目逐项填写。做法很简单:抽10支做空管观察,看内壁是否有可见颗粒、纤维;再抽10支做实采,按标准采血,记录是否能达到标称刻度线,有无回血不畅和负压过强导致的剧烈冲血;之后选其中几支送生化或凝血项目做对比,看同项目的均值和变异系数是否异常一大截。如果发现同批管采血量平均不足10%以上,或者同项目结果变异明显大于室内质控要求,我会直接判定该批“不合格”,厂家要么解释并更换,要么退货。这一步看似“啰嗦”,但可以极大减少使用中才发现问题、被迫大面积重抽血的情况,实打实帮你省下人力和声誉成本。

关键要点二:采血架标准化布局,避免“拿错管”这种蠢错误
在一线我见过太多“拿错管”酿成的事故:血培养错用含抗凝剂管,导致假阴性;凝血项目用成普通促凝管,PT全系乱飞。你靠事后追查几乎不可能完全补救,所以必须从采血架的物理布局上“堵死”这种错误。我推行的做法是:第一,采血架固定位置摆放,不同项目用途的管只允许摆在标记好的槽位,并配色卡和用途文字说明;第二,强制一科一型,不同厂家的同类管不要混搭在同一架上,避免护士凭颜色和记忆出现混淆;第三,给高风险项目(如血培养、凝血、血型交叉配血)单独配专架,物理隔离,减少错拿概率。培训上我会加一个“小考核”:让新护士在不看标签的情况下,仅凭管帽颜色、材质和弹性判断管型,用定时的方式反复练。听起来有点“狠”,但实践证明,经过两周这种训练,拿错管的概率能降到几乎可以忽略不计,这比在事故后开十次会有用得多。
二、针对常见故障设“可视化预警”,让问题暴露在上机之前
采血管最容易引发的故障有三类:溶血、凝块和污染,这三种如果等到仪器报警再处理,已经晚了。我一直强调“可视化预警”,就是在标本接收和分拣阶段,通过肉眼加简单工具,把高风险管先找出来,把损失控制在上机前。比如溶血,我要求接收护士做到“三看”:看血清颜色是否明显粉红或红色;看是否有大量泡沫;看管壁是否有裂痕或冻融痕迹。遇到轻度溶血,我会判断项目类型,诸如钾、LDH、AST等敏感项目建议重采;不敏感项目则在报告单上标记“轻度溶血,结果谨慎解读”。凝块问题则更隐蔽,特别是在抗凝管中,小凝块往往导致仪器探针堵塞或结果不稳定。我给科室配了简单的“手持放大镜+黑色背景板”,接收时快速旋转管身,在黑底下小凝块非常明显,一旦发现直接退回采血点重抽。至于污染,血培养管我要求严格观察液面是否混浊、是否有异物,普通生化管则重点留意管口是否有干涸血迹或被手触碰的痕迹,必要时直接标记为“高风险样本”,先不用于关键决策。
关键要点三:溶血、凝块、污染的分级处理标准
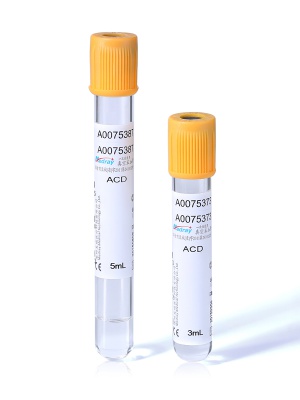
很多科室有个问题:发现溶血、凝块、污染,只靠“经验”处理,结果要么过于宽松,要么过于严格,影响效率。我建议制定一份书面化的《样本质量分级处理表》,让每种问题可视化、可操作。比如溶血可按血清颜色分级:轻度呈微粉红,允许做大部分项目但在报告单上注明;中度呈明显红色,禁止做高敏感项(如钾、LDH、肌红蛋白),建议重采;重度呈深红且不透光,一律退回重抽。凝块可根据数量和大小判断:若在抗凝管内发现任何可见凝块,一律不推荐用于细胞计数或凝血检测,建议重采;非抗凝管出现少量边缘凝块,且与检测项目无直接影响的,可酌情使用,但报告附注。污染方面,则按来源区分:采血口触碰非无菌表面或血培养管瓶塞未规范消毒的,一律按高风险处理,禁止用于微生物判断。这张分级表配合照片示例贴在接收窗口,操作人员按图对照处理,既统一标准,又避免“凭感觉办事”。
关键要点四:善用简单工具,把肉眼检查变成“半自动化”流程
有些人一听“工具”就想到昂贵设备,其实在采血管故障筛查这块,简单工具反而更高效。我推荐两类落地工具:一是“样本质量观察板”,就是一块深色磨砂背景板配上多点LED侧光,接收时将采血管置于板前旋转,溶血程度、微小凝块和污染颗粒都会非常清晰,几乎相当于给肉眼加了个“光学放大版”。这个东西可以自己做,几百块就能搞定。二是“电子记录模板”,利用实验室现有的LIS系统或Excel,把样本质量问题录入为标准字段,比如溶血等级、凝块情况、是否重新采血等,形成可追踪的数据链。这样你能统计出哪位采血人员、哪个时间段、哪种管型问题最多,后续培训和采购就有了精确靶点。很多时候,问题不是你不知道,而是你没数据做证据。一旦数据摆出来,科室的改善动力会强很多,管理也更有底气。
三、用标准化流程和数据闭环,把检测准确性“固化”下来
采血管相关故障最怕的是“今天改,明天忘”,所以必须靠标准化流程和数据闭环来“固化”行为。我在科里推过一套“前处理SOP+事件回溯表”。前处理SOP把每一步写死:采血顺序、混匀次数和节奏、放置时间、离心条件、保存温度、上机时限,每一条都配了“为什么这么做”的简短解释,让年轻人不是机械执行,而是真理解;比如抗凝管混匀不足导致微凝块,从而影响全血细胞计数,这一点我会用真实的对比图让他们记住。事件回溯表则用于记录每一次因采血管问题导致的重采、结果质疑或临床投诉,内容包括管型、批号、采血者、发现时机、影响项目、最终处理结果。这样一来,任何一次事故都不是简单“翻篇”,而是会进入下一轮培训和采购评估中。慢慢的,你会发现几类问题开始大幅减少:错误管型选用、大规模溶血、同一批号集中异常等。检测准确性并不是靠某一个高明操作员,而是靠一整套让每个人“不犯错也不敢犯错”的系统。
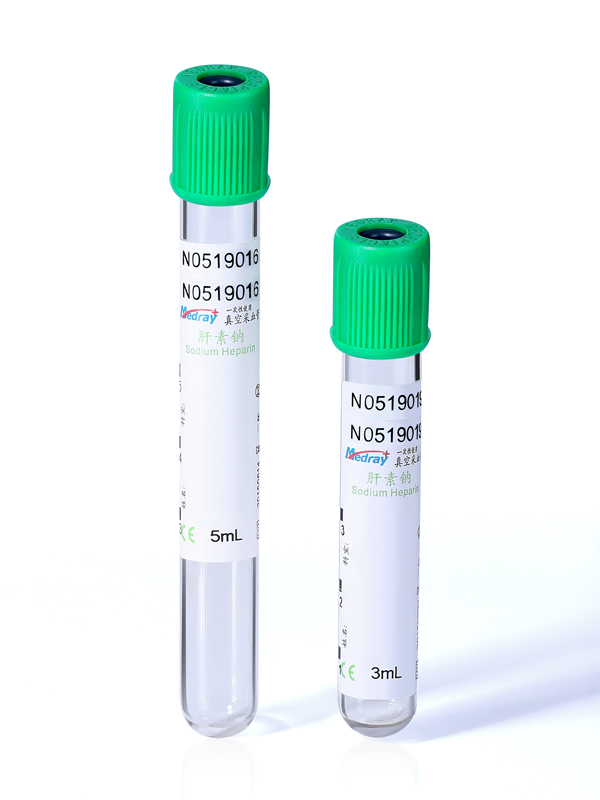
关键要点五:围绕“结果异常”建立问题追踪链
很多人只盯着采血管和前处理,却忽略一个重要抓手:仪器结果本身就是问题的“报警器”。我会要求技术人员对以下几种情况启动“样本质量追踪”:同一批次标本中,某个项目突然普遍偏高或偏低;某个科室、某位医生送检的样本持续出现溶血标记增加;仪器某一通道反复出现堵塞或错误吸样报警。一旦出现这些信号,我们会回溯采血时间、采血地点、管型批号,再结合样本质量记录和到货验证数据,看看是否集中在某段时间换过一批新管,或者某位新护士上岗。这种“反向追踪”很关键,它能发现前期肉眼检查漏掉的问题,尤其是那些轻微但系统性的偏差。举个例子,有一次我们发现某批次钾值集体偏高,最后查到是新到的一批肝素抗凝管添加剂比例异常,肉眼完全看不出来,只能靠仪器结果的“群体异常”来发现。事后我们把这次事件纳入培训案例,大家对批次验证的重要性就再也不敢轻视了。
落地方法示例:建立“采血到结果”全流程质控清单
如果你想快速落地上述做法,可以从一份“采血到结果全流程质控清单”入手。清单分三段:采血端、前处理端、分析端。采血端包括:是否使用正确管型、是否按推荐顺序采集、混匀动作是否规范、止血带时间是否超时等;前处理端包括:是否按规定时间离心、离心参数是否正确、样本保存温度和时限是否合规、是否进行肉眼质量检查并记录;分析端包括:仪器每日开机自检是否完成、质控是否在控、样本上机前条码和体积检查是否正常、异常结果是否进行复查或稀释确认。每一条用简单的“是/否”勾选,并留有备注栏记录问题。开始时可以选一个科室或一个项目先试点,运行一两个月后,根据实际情况删减和优化条目。这样做的好处是,你不用指望一次出台完美制度,而是通过不断迭代,让清单真正贴合你们科室的工作习惯,最后形成一套有血有肉的操作规范。
TAG: 无菌采血管厂家 | 无菌采血管 |


