如何通过评估采血管无菌厂家提高血液检测准确性?
如何通过评估采血管无菌厂家提高血液检测准确性
从业者视角:为什么采血管厂家评估会直接影响结果准确性
我在实验室做质控这些年,一个很深的体会是,很多人只盯着分析仪器和试剂,却忽略了最前端的采血管。说白了,采血管选错了,再好的仪器也救不回来。常见的溶血、凝块、血细胞计数偏低、钾离子偏高、凝血时间异常延长,很多最后追根溯源,都和采血管的材料、添加剂和灭菌工艺有关。要想系统地提高血液检测准确性,第一步不是换设备,而是把采血管无菌厂家的评估做细、做实。我更看重的是三点:一是原材料和灭菌是否稳定可靠,二是添加剂和真空量能不能保证每一管的一致性,三是厂家长期配合度和质量管理习惯好不好。只要这三关守住了,前处理环节的变异会明显下降,质控图也会“乖”很多,这个提升在日常工作里是看得见、摸得着的。
评估采血管厂家的三个关键维度
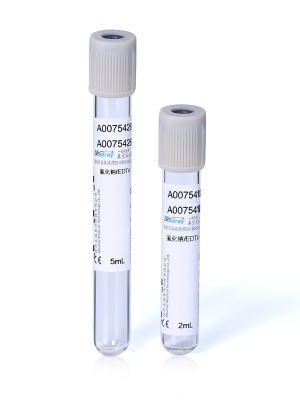
建议一:先看原材料和灭菌工艺,再谈价格
我现在选采血管厂家,第一条就是不先看报价单,而是先要原材料和灭菌相关资料。原材料方面,重点看管体材料是否有合格证明和批次追溯,胶塞、盖子是否有明确的供应商管理记录;最好能看到同一批次原材料对应的物理性能检验报告,比如渗漏率、穿刺性能等。灭菌方面,我会要求厂家提供灭菌方式说明、灭菌验证报告、残留环氧乙烷监测记录,以及无菌检查合格率数据。如果厂家只给一纸合格证,而拿不出批次级的数据,基本上我会保持谨慎。落地做法上,可以把“原材料可追溯”“灭菌验证报告完整”“环氧乙烷残留记录连续三批合格”设成硬性准入项,不满足就不进入小试。别嫌麻烦,这一步过滤掉的,是后面可能无穷无尽的质控和投诉成本。
建议二:把添加剂配方和真空精度当成检测准确性的命门
影响结果偏差最大的,其实是采血管里的“看不见”的东西,也就是添加剂和真空量。以抗凝管为例,枸橼酸钠比例稍微不准,就会直接拖动凝血指标;EDTA过量会造成红细胞收缩、血细胞计数偏低;促凝剂不稳定会导致部分样本凝块、纤维蛋白丝增多。评估厂家时,我会要求提供添加剂配比的工艺控制点和批内均一性数据,比如每批抽检管内添加剂含量的变异系数。真空精度同样关键,负压不足易采血量不足,过大则可加重溶血。这里有一个简单落地方法,实验室可以自行对新厂家的不同批次采血管做随机抽检,用精密天平称量空管与加血后的质量差,估算实际容血量,与标称容积比对,看偏差是否控制在事先约定的范围内。只要这两项稳定,很多莫名其妙的偏差会自然减少。
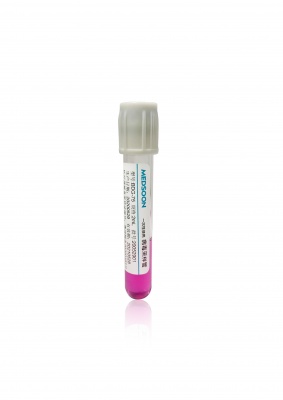
建议三:考察供应稳定性和质量管理习惯,而不是只看一次送样表现
很多厂家送样阶段表现得很“完美”,但是一旦进入大批量供应,就开始频繁更换原材料、代工厂甚至工艺参数,检测结果就会忽好忽坏。因此,我在评估时非常看重厂家是否有成熟的质量管理体系和供应稳定性。可以重点看三个方面:一是是否有完整的批次追溯链,出现问题时多久能给出具体批号和原因分析;二是是否有定期内部质控数据,对关键指标如真空度、添加剂含量、无菌率有持续监测;三是售后响应速度和改进态度。落地操作上,我建议建立一个简单的“厂家评估打分表”,把原材料可追溯、灭菌数据、添加剂一致性、真空精度、供货稳定性、投诉响应时间等做成量化指标,每项设定权重,按事实打分,而不是凭印象拍板。这样既方便年度复评,也便于和采购部门沟通,让“质量”在谈判桌上有具体分数可说。
两个可直接照做的落地方法
方法一:新厂家或新批次的并行试验和偏差分析
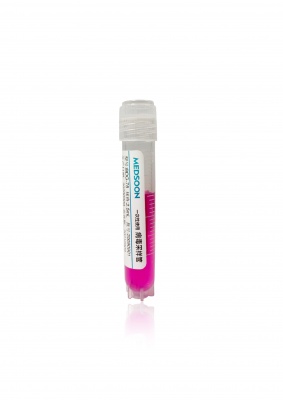
任何一个新厂家或关键型号的新批次采血管,我都会坚持做并行试验,这一步是真正保护结果准确性的最后闸门。操作流程可以这样设计:第一步,选择代表性项目,至少包括血常规、电解质、肝肾功能、凝血项目各一到两个;第二步,选取一定数量的临床真实样本或留存血样,同一受试者同时用现用品牌和待评估采血管采血,保持采血顺序和混匀方式一致;第三步,同一台仪器、同一批试剂、同一时间段内检测,记录两种采血管对应的结果数据;第四步,做配对差值和偏差分析,设置事先约定的可接受偏差范围,比如以生物学变异和室间质评标准为参考。如果发现某类项目偏差方向一致且超过限度,就要追问是添加剂问题、真空问题还是表面处理问题,必要时让厂家参与复核。通过这种并行试验,不仅能筛掉不合格产品,也能把可接受的偏差范围用数据说清楚,避免后面出现争议时各说各话。
方法二:建立简单的“采血管年度复评表”,让评估常态化
一次性的首评远远不够,想真正提高总体检测准确性,更关键的是把厂家评估做成一个年度循环。我的做法是用一个简单的电子表格设计“采血管年度复评表”,内容包括几类信息:一是质量事件记录,如一年内因采血管导致的溶血率升高、凝块比例、真空不足、漏液等问题次数;二是室间质评或内部比对中,怀疑与采血管相关的异常项目次数;三是供货稳定性,如缺货、临时更换批次的情况;四是厂家响应情况,包括问题反馈后答复时间、是否提供书面分析与改进措施。每一项设定分值和扣分规则,例如出现一次严重质量事件直接扣到零分。年底根据得分决定是否继续合作、是否降级为备选厂家。这种工具的好处是操作简单、数据直观,而且能倒逼厂家长期保持稳定,而不是只在首次送样时“表现优秀”。久而久之,你会发现实验室的异常波动少了,很多“玄学问题”其实就是在前端材料层面被消化掉了。
TAG: 采血管红管 | 紫帽采血管 | 红管采血管 | 真空采血管 | 负压采血管 | 负压采血管设备 | 真空采血管设备 | 无菌采血管设备 | 采血管设备 | 采血管紫管 | 采血管绿管 | 微型采血管 | 采血管厂家 | 高血压采血管 | 红盖采血管 | 负压真空采血管 | 白盖采血管 | 抗凝采血管 | 红头采血管 | 紫帽采血管设备 | 血液采血管厂家 | 采血管绿管厂家 | 真空采血管厂家 | 微型采血管设备 | 采血管红管厂家 | 无菌采血管厂家 | 微量采血管设备 | 无菌采血管 | 一次性真空采血管设备 | 血液采血管 | 一次性静脉采血管 | 采血管紫管设备 | 采血管自动贴标 | 负压真空采血管厂家 | 采血管耗材 | 采血管红管设备 | 粉头采血管设备 | 粉头采血管 | 一次性真空采血管 | 抗凝采血管厂家 | 血液采血管设备 | 采血管蓝管 | 采血管紫管厂家 | 负压真空采血管设备 |


