了解白盖采血管设备的标准为何至关重要?
了解白盖采血管设备的标准为何至关重要
从一线经验看标准的重要性
我在实验室和临床一线干了很多年,见过太多问题都是从一支看似普通的白盖采血管开始的。说句实在话,很多同事刚入行时,习惯把白盖采血管当成便宜耗材,只关心有没有货、好不好抽,却很少认真翻过一次产品标准和说明书。结果就会出现标本凝血时间不稳定、溶血率偏高、检测结果重复性差等问题,追根溯源才发现是采血管本身的添加剂、材料和负压与现有仪器不匹配。如果你不了解它的注册标准、适用项目范围、储存和有效期要求,那么再严谨的操作习惯也可能被设备本身拖后腿。对白盖采血管设备标准的熟悉程度,决定了你能不能在问题刚冒头时就发现异常,是被动救火还是主动预防,也是科室是否能通过质控评审和外部督查的关键一环。
三个必须掌握的关键要点
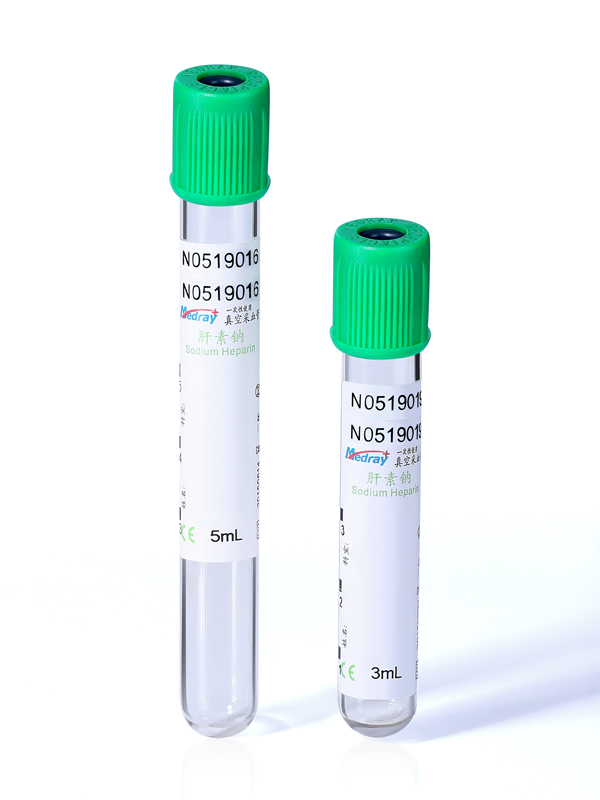
要点一:把白盖采血管当作医疗器械而不是耗材
很多科室在采购和使用白盖采血管时,只盯着价格和供货稳定性,这在我看来是典型的风险源。白盖采血管本质上是直接进入人体、直接影响检验结果的医疗器械,它的注册证信息、执行标准、适用样本类型、是否一次性使用、是否含促凝剂或分离胶等,都需要像审核大型设备一样去看。实际操作中,我会要求物资和检验双部门共同参与准入评估,对新品牌必须先做小批量比对试验,至少验证常规生化、免疫项目的结果一致性和标本稳定性,再考虑全面替换。只有把它当设备管理,建立台账、记录批号、追踪不良事件,你在出现结果偏差、病区投诉或院感事件时,才能有据可查,有底气说清楚哪些问题与采血管有关,哪些与操作有关。
要点二:紧扣标准中的关键技术参数
白盖采血管设备标准写得很厚,但真正决定风险的技术点其实就几个,我一般会盯住这几个参数不放。第一是管体与胶塞材料,对耐压性、密封性以及与血液成分的相容性影响很大,直接关系到是否会漏气、是否容易溶血。第二是预置负压和标称采血量,如果与实际常用针头规格、采血姿势不匹配,很容易出现采血不足、大量气泡或者回流速度过快等情况。第三是灭菌方式和无菌保证期,尤其是在高强度抽检、频繁搬运的场景下,包装破损和批次混用都可能带来院感隐患。理解这些标准并体现在采购技术条款和入库验收细则里,比泛泛而谈質量优先重要得多,也更能真正降低日常工作中的隐性风险。
要点三:把标准转化为流程和记录
标准如果只停留在纸面上,最多是检查时好看,真正能救场的是流程和记录。我的做法是,把白盖采血管的关键标准拆成多个环节嵌入日常工作,例如采购阶段有技术审核表,入库有外观和批号核对表,临床发放有批次登记,使用后出现溶血增加或疑似凝血异常时有事件上报和样本回溯表。这样做的好处有三点,其一是每个环节有人负责,而不是出了问题大家都说不清。其二是一旦发现某一批次疑似有问题,可以快速锁定范围,通知相关科室停用并更换。其三是长期积累的数据可以反向指导采购和供应商管理,哪些品牌在本院环境下稳定可靠,哪些经常引发隐性故障,一目了然。说白了,就是用流程把标准固化下来,用记录让每一次小异常都能被看见。
落地方法与工具建议
如果你想在科室里真正把白盖采血管设备标准落到实处,我建议至少先做两件事。第一,建立一份简单但严谨的白盖采血管准入和验收清单,把前面提到的材料、负压、执行标准、适用项目、灭菌信息、有效期和批号记录等项目列进去,新品牌上线或新批次大批量入库时必须逐项打勾并留底,可以用科室现有的电子表格工具维护,定期备份并打印一部分存档。第二,在日常工作中设定一个可操作的异常触发点,例如某一类项目溶血率连续几日明显升高,或者特定病区反馈抽血困难明显增加时,由检验科启动一个小范围排查,优先检查采血管批次和保存条件,再看操作流程,并把排查过程记录在统一模板里。很多人觉得这类表格和记录很琐碎,但一旦你经历过一次因为采血管质量问题导致大批结果复查、甚至需要召回病人的事件,就会明白这些工具实际上是在帮你提前把风险挡在门外。
TAG: 采血管红管 | 紫帽采血管 | 红管采血管 | 真空采血管 | 负压采血管 | 负压采血管设备 | 真空采血管设备 | 无菌采血管设备 | 采血管设备 | 采血管紫管 | 采血管绿管 | 微型采血管 | 采血管厂家 | 高血压采血管 | 红盖采血管 | 负压真空采血管 | 白盖采血管 | 抗凝采血管 | 红头采血管 | 紫帽采血管设备 | 血液采血管厂家 | 采血管绿管厂家 | 真空采血管厂家 | 微型采血管设备 | 采血管红管厂家 | 无菌采血管厂家 | 微量采血管设备 | 无菌采血管 | 一次性真空采血管设备 | 血液采血管 | 一次性静脉采血管 | 采血管紫管设备 | 采血管自动贴标 | 负压真空采血管厂家 | 采血管耗材 | 采血管红管设备 | 粉头采血管设备 | 粉头采血管 | 一次性真空采血管 | 抗凝采血管厂家 | 血液采血管设备 | 采血管蓝管 | 采血管紫管厂家 | 负压真空采血管设备 |


