选择负压采血管厂家的时候,需要了解哪些认证标准?
选择负压采血管厂家时,这些认证标准我一定会先看
先说清楚:为什么认证比价格更关键
我在医疗耗材和体外诊断这一行干了十几年,负压采血管见过的厂家和事故都不少。很多人选供应商时,只盯着单价和交期,结果遇到批次不稳定、溶血、真空不足、硅化剂脱落,最后都砸回到临床科室和检验科身上。说白了,负压采血管是直接接触血样的医疗器械,一旦出问题,轻则重复采血、投诉不断,重则影响检验结果,误判病情,甚至引发院内感染和大面积召回。我自己选厂家的第一反应,从来不是问多少钱,而是先翻认证和注册资料,看它是不是在监管体系里站得住脚,质量体系是不是真正跑起来了。这套习惯听上去有点啰嗦,但实战中帮我躲开了不少坑,也让我敢推进长期框架协议,因为心里有底,知道这些管子是经得起抽检和事故追溯的。
3〜6条我实战中最看重的核心建议
从实战经验讲,负压采血管厂家认证很多,名字也容易把人看晕,但真正影响你临床使用安全和后续追责的,其实就几条主线。我一般会把它拆成三层:第一层是法规合规,至少要有合法的生产资质和注册证;第二层是质量体系,重点是是否建立符合医疗器械要求的体系,并且在持续运转;第三层是产品相关标准,比如生物相容性、无菌控制、真空保持和稳定性验证等。落地时,我会按这三层罗列一个清单,让每个厂家自己填资料,再结合抽查和现场评估打分,这样就不是拍脑袋,而是有证据、有记录地选。下面这几条,是我给团队最常强调、也最容易直接落地的关键点:
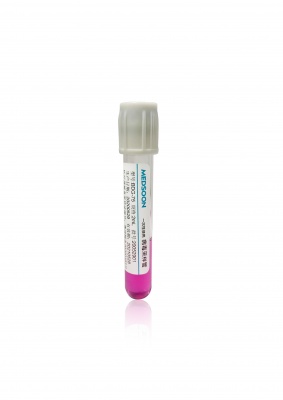
- 必须查清该厂家是否有合法的医疗器械生产许可证和对应规格的注册证。
- 优先选择通过医疗器械质量体系认证的厂家,例如以 ISO 13485 为核心的体系。
- 确认负压采血管的关键安全标准,例如生物相容性、无菌、真空保持、加速老化验证是否齐全。
- 如果涉及出口或跨院采购,看清是否有欧洲 CE、美国 FDA 等目标市场的合规基础。
- 核实批号追溯、检验报告和变更控制机制,确保出问题时能追得上去、查得清责任。
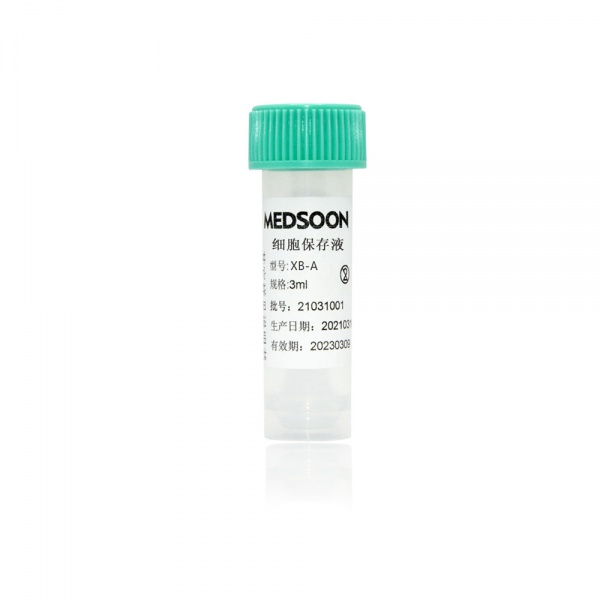
关键认证标准:我会这样一条条核对
基础合规和质量体系:没这一步,其他都免谈
第一步我一定看基础证照,这块别嫌麻烦。对国内厂家来说,至少要有医疗器械生产许可证、营业执照,以及每一类负压采血管对应的医疗器械注册证,注册证备案人、生产企业、规格型号要和你实际采购的完全对应。很多人只看一张复印件就算数,结果后面发现实际供货的是挂靠生产,这种风险非常大。在质量体系方面,我会优先选择有 ISO 13485 认证的厂家,它是医疗器械行业最基本的质量管理框架,比普通的 ISO 9001 要求更贴近法规;如果对方还做出口,顺带会看有没有通过相关国家或地区的审查,例如带医疗器械范围的 GMP 要求。真正靠谱的厂家,不会只给你一张证书照片,而是能提供在有效期内的证书、认证机构信息,甚至愿意开放部分内审、管理评审记录供你现场审核。
产品安全与性能相关标准:盯住和血样直接相关的几件事
通过了基础合规,只能说明这家厂有资格生产,离“敢用”还差一截,我会再往下看产品层面的标准和验证。负压采血管首先要过生物相容性这一关,常见会参考如 ISO 10993 系列方法,核查是否做过细胞毒性、皮肤刺激等试验,避免材料析出物影响患者安全。其次是洁净和无菌控制,看是否有无菌或无菌保证水平相关验证报告,以及洁净车间级别和环境监测记录。真空保持和抗凝剂稳定性,是采血管最容易被忽视却常出事故的地方,我会要求查看加速老化和真实时间稳定性的数据,看在有效期末端还能否保证抽取体积和血液状态稳定。最后是包装标签和说明书的符合性,包括批号、有效期、灭菌方式、储存条件等,这些既关系到院内管理,也关系到后续一旦追责时能否说得清楚。
两个好用的落地方法和工具
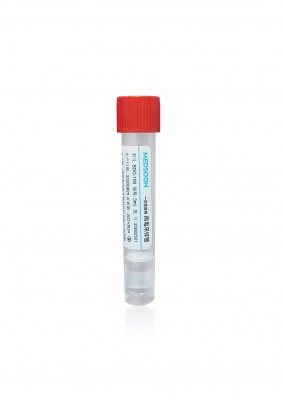
方法一:用官方数据库核实注册与认证真伪
纸面资料谁都会做,想要少踩坑,我建议一定把官方数据库用起来。国内可以直接上国家药监局的信息服务平台,用企业名称或注册证编号查询,核对注册证是否在有效期内,生产地址是否一致,获批产品的名称和规格是否包含你要买的那几类管子;如果对方号称有出口资质,可以抽样到目标国家或地区的官方数据库,比如查看是否在相关监管机构网站上能查到对应产品或企业信息。和厂家沟通时,我会让他们先提供注册证编号和认证证书编号,然后由我们自己去系统里查,这样既节省时间,又能测试一下对方的配合度和透明度。说白了,这一步就是用公开信息帮自己做第一轮筛查,把明显不合规或信息前后矛盾的厂家先排掉。
方法二:做一个简单打分表,把“感觉”变成数字
第二个我常用的小工具,就是给团队做一份供应商打分表,用表格把认证和标准拆成几项,让每个厂家根据材料和现场审核情况打分。比如分成法规合规、质量体系、产品验证、现场管理四大块,每块下面列出刚才说的关键点,如生产许可证和注册证、质量体系认证、生物相容性和无菌验证、真空保持和稳定性数据、批次追溯能力等,再给每项设置权重。采购、质管、检验科三方一起参与打分,最后算出一个综合分。这样一来,选厂不再是某个人的主观印象,而是可以回头复盘的决策过程,也方便后续年度复审时对比分数变化,判断这个厂家是越来越稳,还是在下滑。工具很简单,用电子表格就够,关键是把要点列清楚、打分标准讲透,团队都按同一套尺子来量。
结语:先盯住认证,再谈价格和关系
回头看我这些年的经验,选择负压采血管厂家,认证和标准不是锦上添花,而是“能不能用”的生死线。只要把基础合规、质量体系、产品安全标准和追溯能力几件事按清单逐条核对,再配合官方数据库和打分表这样的简单工具,大部分坑在前期就能看出来。后面再去谈价格、供货周期、账期和增值服务,你会发现对话位置完全不一样,心里也更有底。最后提醒一句,无论厂家多熟、人情多深,认证和验证资料一定要自己亲眼看、亲手查、认真留存记录,这既是对患者负责,也是给你和医院留一条安全的退路。
TAG: 采血管红管 | 紫帽采血管 | 红管采血管 | 真空采血管 | 负压采血管 | 负压采血管设备 | 真空采血管设备 | 无菌采血管设备 | 采血管设备 | 采血管紫管 | 采血管绿管 | 微型采血管 | 采血管厂家 | 高血压采血管 | 红盖采血管 | 负压真空采血管 | 白盖采血管 | 抗凝采血管 | 红头采血管 | 紫帽采血管设备 | 血液采血管厂家 | 采血管绿管厂家 | 真空采血管厂家 | 微型采血管设备 | 采血管红管厂家 | 无菌采血管厂家 | 微量采血管设备 | 无菌采血管 | 一次性真空采血管设备 | 血液采血管 | 一次性静脉采血管 | 采血管紫管设备 | 采血管自动贴标 | 负压真空采血管厂家 | 采血管耗材 | 采血管红管设备 | 粉头采血管设备 | 粉头采血管 | 一次性真空采血管 | 抗凝采血管厂家 | 血液采血管设备 | 采血管蓝管 | 采血管紫管厂家 | 负压真空采血管设备 |


