如何通过选择适合的负压真空采血管满足不同实验需求?
如何通过选择适合的负压真空采血管满足不同实验需求
先厘清需求:不是所有血样都能靠“万能管”解决
我在实验室带新人时,第一件事就是打破“万能采血管”的幻想。不同的实验目的,对抗凝剂、添加剂、血清/血浆类型和稳定性要求完全不同,如果只盯着颜色或习惯用法,很容易踩坑。临床常规、生化免疫、分子诊断、凝血、微量元素、药物浓度监测,这几个大方向,对采血管的要求差异巨大。比如做PCR,对DNA/RNA完整性和抑制物极度敏感,这时选择含有EDTA但不含干扰表面活性剂的管子比什么都重要;而做凝血功能,则必须用标准配比的枸橼酸钠管,并且管内液体体积要与采血量严格匹配,否则PT/APTT会整体偏长或偏短。我的经验是,先按“检测目的→标本形态(血清/血浆/全血)→添加剂类型→体积和材质”这条路径梳理需求,而不是“有什么颜色就用什么管”。当你能在开单或设计实验方案时,就脑内自动匹配到对应管型,样本重采率和无效结果会明显下降,这一点在高通量实验室尤为明显。
关键要点1:按“检测目的→标本形态→添加剂”倒推采血管
实操时,我会要求同事先问自己三个问题:第一,我要测的是“什么成分”(细胞、蛋白、凝血功能、核酸、微量元素还是药物浓度);第二,我需要的是“血清、血浆还是全血”;第三,哪些添加剂绝对不能干扰目标检测。比如做流式细胞术,需要有完整细胞形态和可染色表面抗原,就优先选K2EDTA抗凝全血,避免肝素等对部分荧光标记的潜在影响;做血清学和大部分生化免疫,反而需要凝固后取血清,此时促凝剂+无抗凝的血清管更合适。很多人只看说明书上的“适用于生化、免疫”,但不去对照自己具体项目,例如补体检测、某些激素或细胞因子对离心时间和室温放置非常敏感,就需要选择带分离胶、促凝剂优化过的管型,并在科室内统一离心窗口。我的独家小技巧是:做一张“科室检测-用管对照表”,按项目精确指定管型和顺序,让用管从“拍脑袋”变成“查表执行”。
从颜色到添加剂:搞清每种管子的真正用途
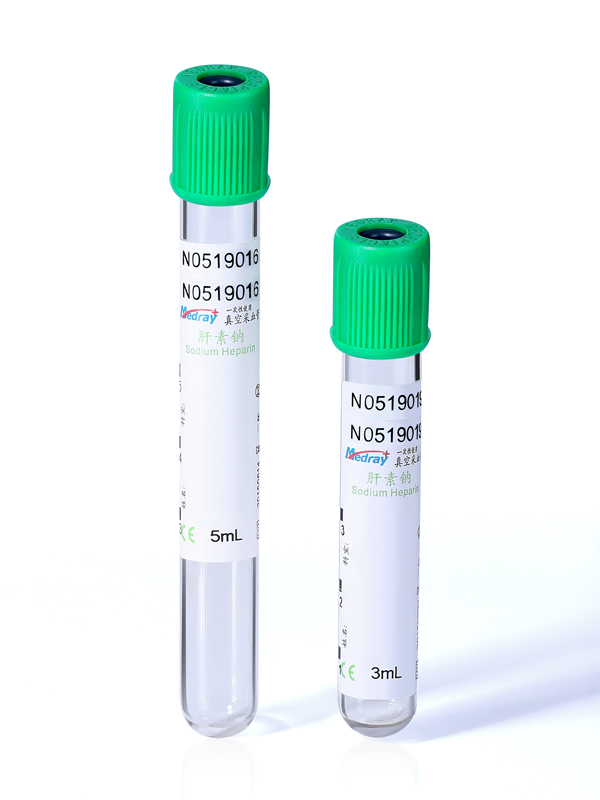
颜色只是便于识别的外壳,本质是管内添加剂和材质在起作用。负压真空采血管的常见类型,基本可拆解为几类:无添加剂或含促凝剂的血清管(多为红头或金头,金头常带分离胶);EDTA抗凝全血管(常见紫头,用于血常规、血型、部分分子检测);肝素锂或肝素钠抗凝管(绿头,多用于急诊生化、部分电解质和血气);枸橼酸钠管(蓝头,用于凝血功能);含氟化钠-柠檬酸钾等的糖代谢保护管(灰头,用于血糖、乳酸等)。同一颜色下,不同厂家在添加剂量、喷涂工艺、分离胶配方上都有差异,性能可以相差非常大。比如分离胶的亲脂性不同,会对某些小分子药物或疏水性激素产生吸附,导致检测偏低;有些促凝剂过强或不均匀,会产生微凝块,影响免疫比浊结果。我的做法是:新采购或更换品牌前,设计一批平行对比样本,用关键项目做性能验证,而不是“换管不换验证”。
关键要点2:一定要明确每种颜色背后的添加剂和适应证
在培训中,我会要求大家不仅记“紫头=EDTA”,而是要清楚“EDTA会螯合二价金属离子”,所以不适合测钙、镁、锌等微量元素,也会影响某些金属酶的活性;肝素会激活抗凝血酶,对凝血项目有显著干扰,但更适合用于血气、电解质,因为对细胞损伤相对较小。枸橼酸钠管必须按1:9配比采血,采不满会稀释血浆,导致凝血时间假性延长。很多临床科室出现奇怪结果,追根究底就是“拿错管”或“同一颜色不同配方”惹的祸。我的建议是,科室内应制作简明的“颜色-添加剂-禁忌项目”卡片贴在采血处和检验科标本接收处,例如:紫头EDTA“禁用于微量元素、生化钙镁、凝血功能”;金头分离胶“慎用于药物浓度监测、某些激素项目”。这样的可视化提醒,远比一堆文件更能改变日常行为。
体积、材质和负压:别小看采血量与管体本身
很多人只看“管的颜色”,忽略了体积、管材和负压设计。负压真空采血管是按目标采血量校准的,采不满会改变血液与添加剂比例,尤其是枸橼酸钠和EDTA,误差可以直接反映在检测结果上。儿科、血容量不稳定患者、ICU小体重病人,如果你拿成人常规体积去抽,很容易导致“半管血”。我自己在设计流程时,习惯按人群和项目区分常规管、小容量管和微量管,尽量避免“能采多少算多少”的随机操作。材质方面,玻璃管和塑料管(PET)在表面活性、吸附特性上都不同,微量元素检测应优先选择经特殊处理、金属背景极低的专用管,而不是随便用一支普通真空管。对于高灵敏度免疫项目,某些塑料增塑剂也有可能成为干扰源。负压强度还会影响溶血风险,静脉细、血流慢的患者,过大的负压会显著增加溶血率,此时可以考虑低负压版本或微负压管配合温和采血动作。

关键要点3:体积不匹配和溶血是最常见、也最好预防的问题
我见过不少实验室,凝血项目总是出现“复查正常”的情况,追查后发现大量标本是“半管枸橼酸钠”,导致结果假性延长。解决方案其实很务实:第一,在采血条形码上增加“必满管”提示,对于凝血、血气等项目,系统中不允许登记“采不满”的解释;第二,为儿科和低体重量患者准备专用小体积管,同时按项目重新校准血液与抗凝剂比例。溶血方面,除了穿刺技术,负压过大和摇晃过猛也是主因。可以要求护士或采血技师在抽血后,按“轻轻颠倒混匀8-10次,不剧烈上下摇晃”的标准操作执行,并在培训中通过对比照片展示溶血对结果的影响,让大家真正重视细节。长期下来,你会发现溶血率和不合格标本率明显下降,这比事后解释和重采更省时省力。
顺序与流程:用好“采血顺序表”和LIS规则引擎
负压真空采血的顺序不只是形式,它直接关系到添加剂交叉污染风险。比如如果先抽EDTA管再抽血清管,少量残留在针头或软管里的EDTA就可能被带入后续管中,导致钙明显偏低;先抽肝素再抽某些免疫或凝血项目,也存在类似问题。因此,“先血培养→枸橼酸钠→无抗凝/促凝血清管→微量元素专用管→肝素→EDTA→糖代谢保护管”这样的大致顺序是值得坚持的。但现实中,靠记忆和口头强调往往不可靠,我更推崇用系统和流程来兜底。比如在LIS中按项目自动生成采血顺序,并在采血打印标签上,用明显的序号标注“1/3、2/3、3/3”,强制执行顺序采血;同时,在检验科接收端,对典型错误组合(如EDTA后接血清做钙)设定自动质控警告。
关键要点4:用数字化工具把“正确顺序”变成“无法做错”
单靠记忆和纸质培训难以长期维持高质量,我更推荐的落地方法是:一,在LIS/HIS或采血条码系统中配置“采血管推荐和顺序规则”,医生开单时只选项目,由系统自动匹配管型和数量,采血端打印出的标签已经包含正确顺序和颜色提示;二,在接收端配置“标本前质控规则”,比如当某些项目与不合适的管型组合出现时,系统弹窗提示“管型不匹配,建议退回重采”,必要时甚至禁止继续上传结果。这样,前端如果拿错管,后端能及时拦截。对规模较小、系统功能有限的实验室,也可以用一个简单的工具落地:制作一张固定模板的“采血管选择与顺序表”,贴在采血室显眼位置,并按月份轮流由一名质控负责人抽查实际执行情况。只要有反馈闭环,规范是能逐步做实的。
两个可落地的方法:用“对照表+验证”把选择做扎实
结合这些年的经验,我最常向其他实验室推荐的两个方法,一个是“科室定制的采血管选择对照表”,另一个是“新管型或新项目的验证流程”。对照表的核心不是罗列全部理论,而是针对本院、本实验室的项目清单,逐项明确“推荐管型、可替代管型、禁用管型”和“是否必须满管、是否必须分离胶”等信息。一旦制定好,就把它内嵌到医生开单小贴士、护士培训教材和检验科SOP中,让所有人用的是同一套“地图”。第二个方法,是所有重大变更前必须做小规模验证:例如更换分离胶管品牌、新增药物浓度监测项目、扩展高灵敏度激素检测等,预先选取20–40个代表性样本,分别用新旧管型采集,做平行对比,关注偏倚、变异和溶血率等指标。如果没有这个环节,很难发现那些只在特定项目和特定人群中才会暴露的细微干扰。我自己的体会是:只要把“选对管、用对管、验证管”变成固定动作,而不是临时灵感,负压真空采血管不仅能满足不同实验需求,还能明显提升整个实验室的结果可靠性和沟通效率。
关键要点5:从“用哪个管”升级为“整体标本前管理”
严格来说,如何选择合适的负压真空采血管,只是标本前管理的一部分。真正成熟的做法,是把“管型选择、采血顺序、采血量控制、混匀和离心条件、运输和存储时间”视为一个完整链条,用制度、培训和数字化工具一起去支撑。我的个人建议是:一,先用上面提到的“对照表+顺序规则+关键项目验证”三件套,解决80%的显性问题;二,后续每季度统计一次“溶血率、不合格标本率、因用管错误导致的退样和复查率”,用数据驱动改进,而不是只在出问题时临时开会“背锅”。这样做下来,前端护士不再恐惧“检验科老是嫌弃采血不规范”,检验科也少了大量解释工作,医生端看到的结果更稳定,整个体系才算真正把采血管当成了“质量管理工具”,而不是一支一次性耗材。
TAG: 采血管红管 | 紫帽采血管 | 红管采血管 | 真空采血管 | 负压采血管 | 负压采血管设备 | 真空采血管设备 | 无菌采血管设备 | 采血管设备 | 采血管紫管 | 采血管绿管 | 微型采血管 | 采血管厂家 | 高血压采血管 | 红盖采血管 | 负压真空采血管 | 白盖采血管 | 抗凝采血管 | 红头采血管 | 紫帽采血管设备 | 血液采血管厂家 | 采血管绿管厂家 | 真空采血管厂家 | 微型采血管设备 | 采血管红管厂家 | 无菌采血管厂家 | 微量采血管设备 | 无菌采血管 | 一次性真空采血管设备 | 血液采血管 | 一次性静脉采血管 | 采血管紫管设备 | 采血管自动贴标 | 负压真空采血管厂家 | 采血管耗材 | 采血管红管设备 | 粉头采血管设备 | 粉头采血管 | 一次性真空采血管 | 抗凝采血管厂家 | 血液采血管设备 | 采血管蓝管 | 采血管紫管厂家 | 负压真空采血管设备 |


